Pojďme nyní spojit makroskopické vlastnosti materiálu (jeho pevnost a pružnost) s jeho mikroskopickou strukturou. Velmi záleží na uspořádání jednotlivých atomů a na vazbách mezi nimi. Současná technika nám umožňuje podívat se dovnitř různých látek, což nám velmi napomáhá k tomu, abychom porozuměli, jaké jsou jejich vlastnosti.
Materiály pod mikroskopem

Zdroj

Zdroj

Zdroj
Zdroj

Zdroj
Podívejte se také na nasledující dvě videa:
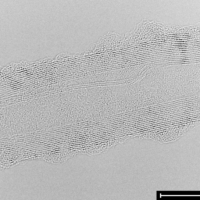
Buňky můžeme vidět i v optickém mikroskopu. Co když ale struktura materiálu není vidět tak snadno? V tom případě máme k dispozici výkonnější mikroskopy.
Skenovací elektronový mikroskop (SEM) nebo transmisní elektronový mikroskop (TEM)
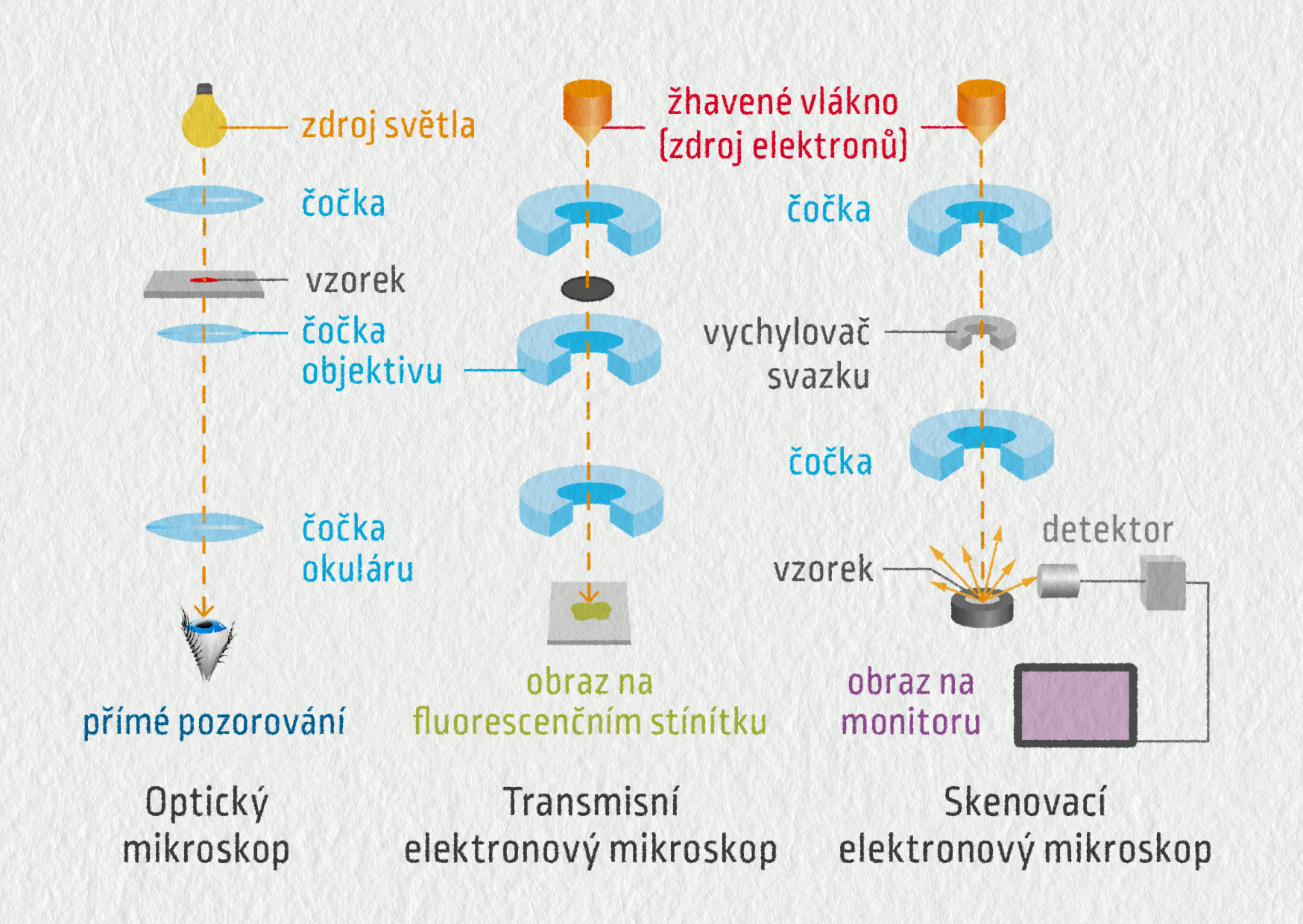
Zdroj
Princip transmisního elektronového mikroskopu (TEM z anglického transmission electron microscope) je velmi podobný principu optického mikroskopu. Svazkem urychlených elektronů prosvítíme zkoumaný vzorek a obraz pak soustředíme pomocí elektromagnetických čoček na fluorescenčním stínítku nebo na monitoru počítače.
V případě skenovacího elektronového mikroskopu (SEM z anglického scanning electron microscope) soustředíme svazek elektronů do jednoho bodu vzorku a tímto svazkem skenujeme („prohlížíme“) určitou oblast na jeho povrchu. Přitom detektorem zachycujeme rozptýlené a sekundární elektrony a vytváříme obraz na monitoru počítače.
Mikroskop atomárních sil (AFM)
Princip AFM mikroskopu (AFM z anglického atomic force microscope) je zcela jiný. Velmi ostrý hrot sondy se pohybuje po povrchu vzorku nebo těsně nad ním a detekuje se vzájemná meziatomová přitažlivost. Aby nedošlo k poškození hrotu, používá se i bezkontaktní režim, kdy se nosník sondy rozkmitává a měří se velikost jeho amplitudy, která závisí na vzdálenosti hrotu a vzorku. Takto mapujeme povrch vzorku.
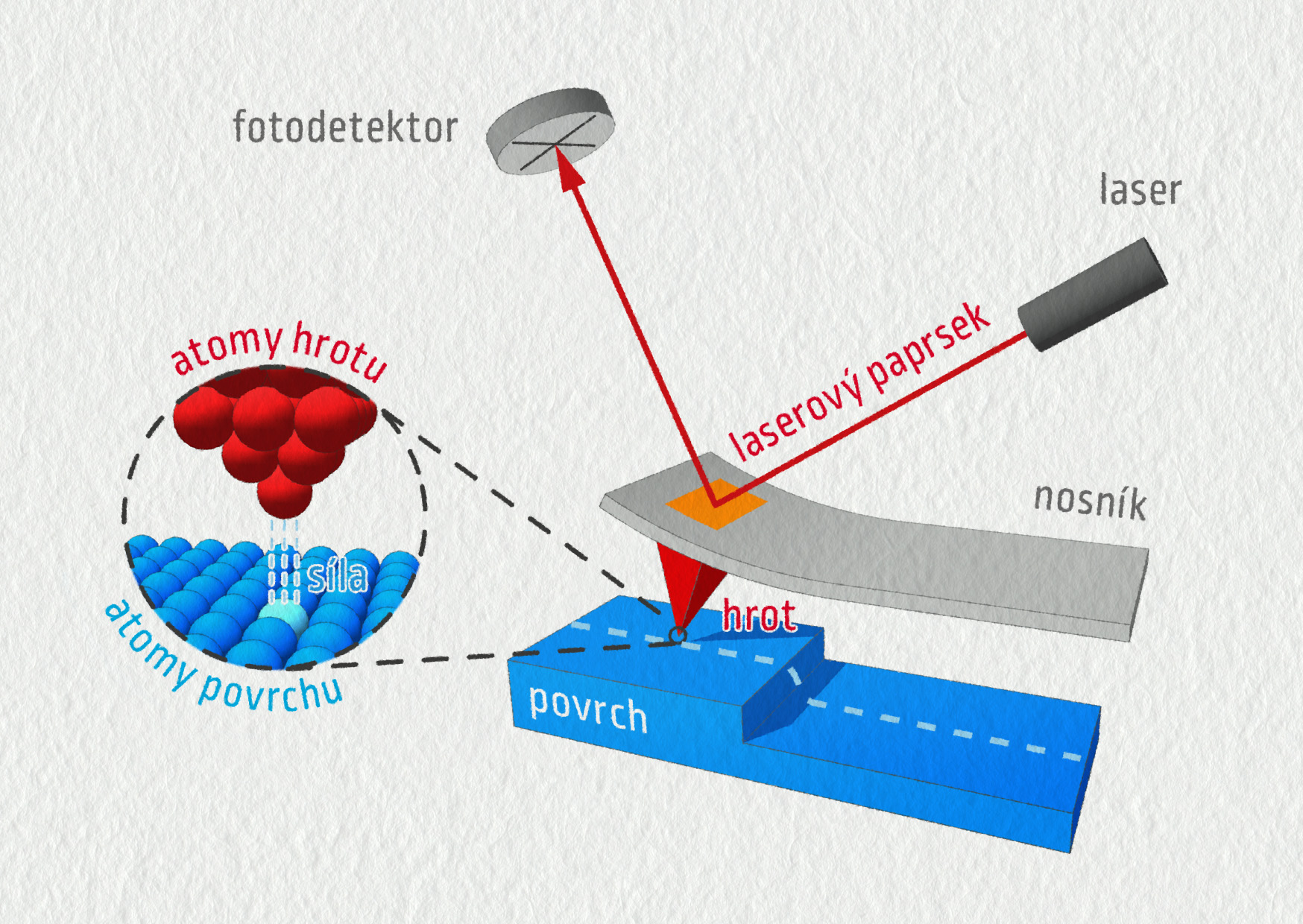
Zdroj
Tyto přístroje nám ovšem ukazují převážně pouze povrch materiálu. Když se chceme podívat na jeho vnitřní strukturu, musíme použít jinou techniku – rentgenovou strukturní analýzou nebo třeba elektronovou difrakci pomocí TEM. Tyto metody totiž umožňují podívat se, jak jsou uspořádány atomy uvnitř hmoty. A častokrát je to jinak než na jejím povrchu.
Krystalová mřížka
Jak vznikají pevné látky? K vytvoření pevné látky dochází většinou při ochlazování kapaliny (například při tuhnutí vody v mrazáku). Vznikne mnoho zárodků krystalů, které se zvětšují a spojují. Oblast látky, která je tvořena mnoha malými krystaly, se označuje jako polykrystalická.

Zdroj
Za vhodných podmínek (například při desublimaci vodní páry v atmosféře) může vzniknout jen jeden větší krystal. Oblast látky, kterou tvoří jeden velký krystal, se nazývá monokrystalická.

Zdroj
Jestliže pevná látka nemá pravidelnou strukturu (například polyethylen, tvořený velmi dlouhými molekulami), nazýváme ji amorfní.
Krystalické a amorfní látky

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj
Jak vypadají vnitřní struktury těchto látek? Podívejme se například na křemen – SiO2, který je v zemské kůře hojně zastoupen a tvoří součást různých hornin, třeba žuly nebo pískovce. Na následujícím rovinném modelu vidíme, že atomy křemíku (zelená barva) a kyslíku (červená barva) jsou zcela pravidelně uspořádány. Toto uspořádání se opakuje periodicky v rámci celého krystalu či krystalových zrn v polykrystalické látce. V látkách amorfních toto pravidelné uspořádání nalezneme jen těžko.
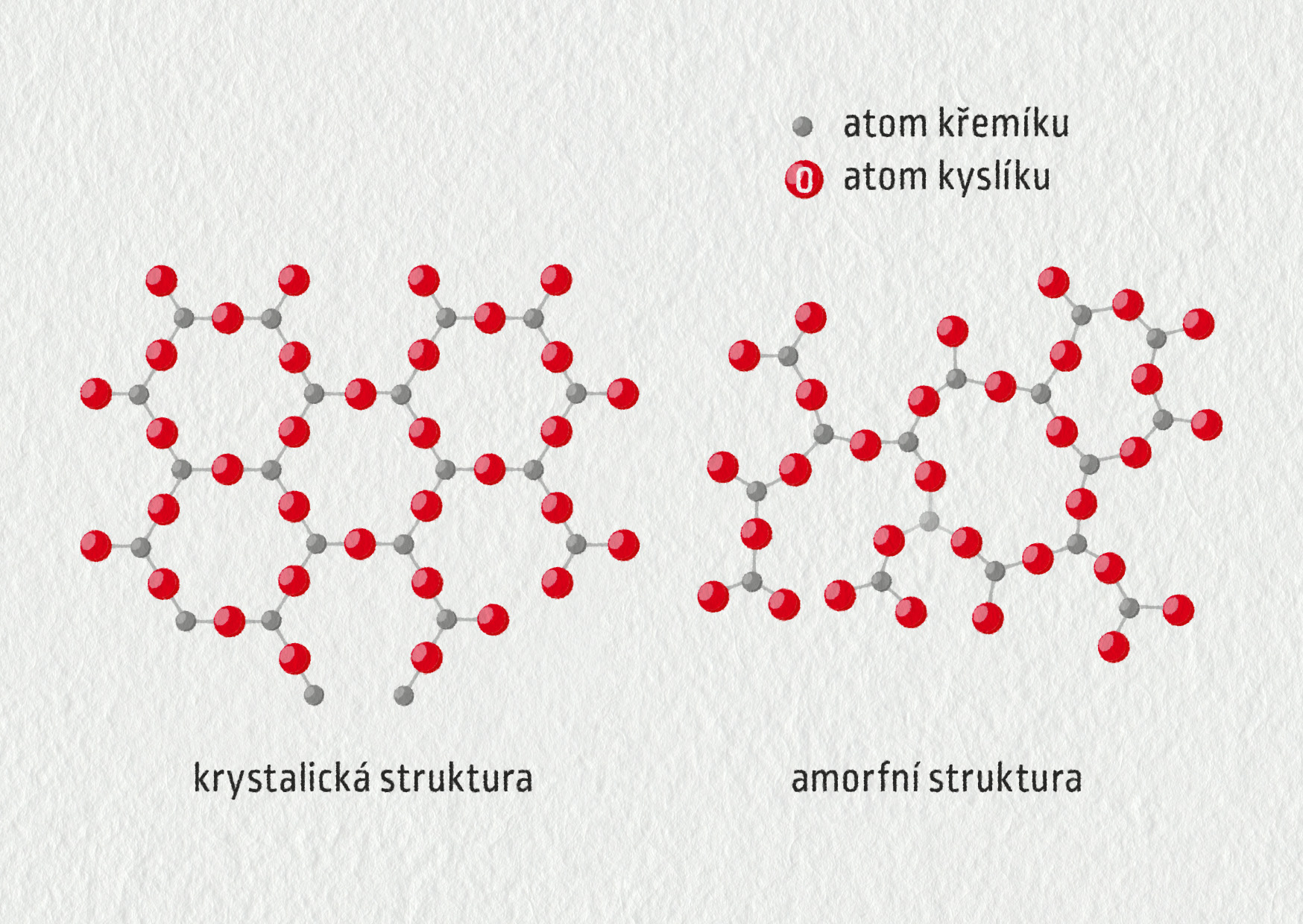
Zdroj
Protože v krystalických látkách najdeme pravidelné uspořádání částic (atomů, molekul, iontů) ve velkých oblastech, hovoříme o tzv. krystalové mřížce, zatímco amorfní látky takové uspořádání nevykazují.
Krystalová mřížka vznikne tak, že prostor rozdělený na jednotlivé buňky (můžeme si je představit jako malé krychličky vymezující část prostoru) osadíme jednotlivými částicemi. „Motiv usazení“ částic v jedné takové krychličce se pravidelně opakuje a vzniká krystalická látka.
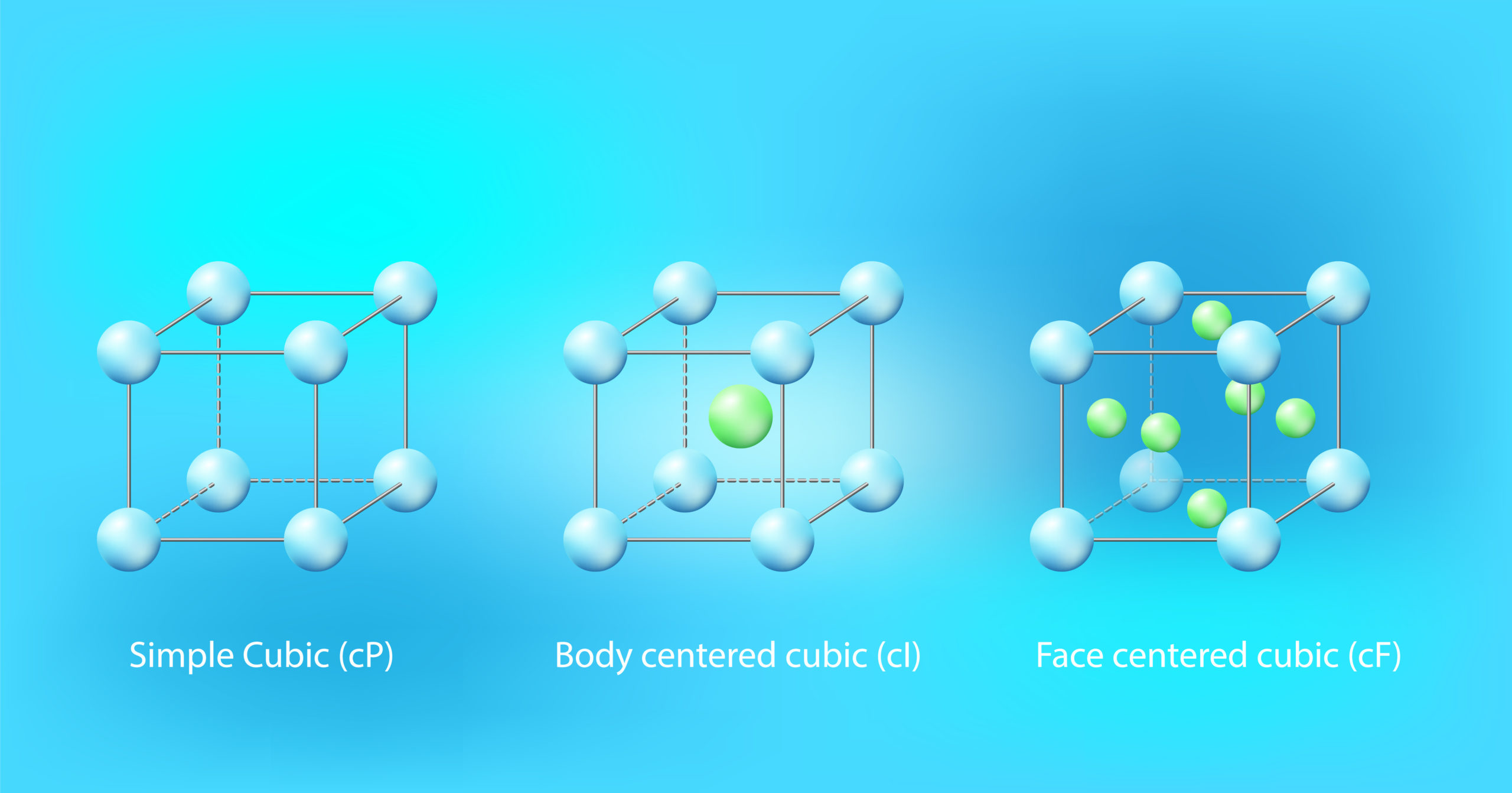
Zdroj
Krystalová mřížka a vlastnosti materiálů
Typ krystalové mřížky a přítomné poruchy mají zásadní vliv na fyzikální vlastnosti materiálů. Známým příkladem je uhlík, který za normálního tlaku a teploty může existovat ve formě velmi tvrdého diamantu (diamantová mřížka = FCC mřížka se 2 atomy v každém uzlovém bodě) a velmi měkkého grafitu (hexagonální mřížka). Kromě toho tvoří atomy C další struktury: nanotrubky, fullereny (molekuly ve tvaru fotbalového míče) a grafen.
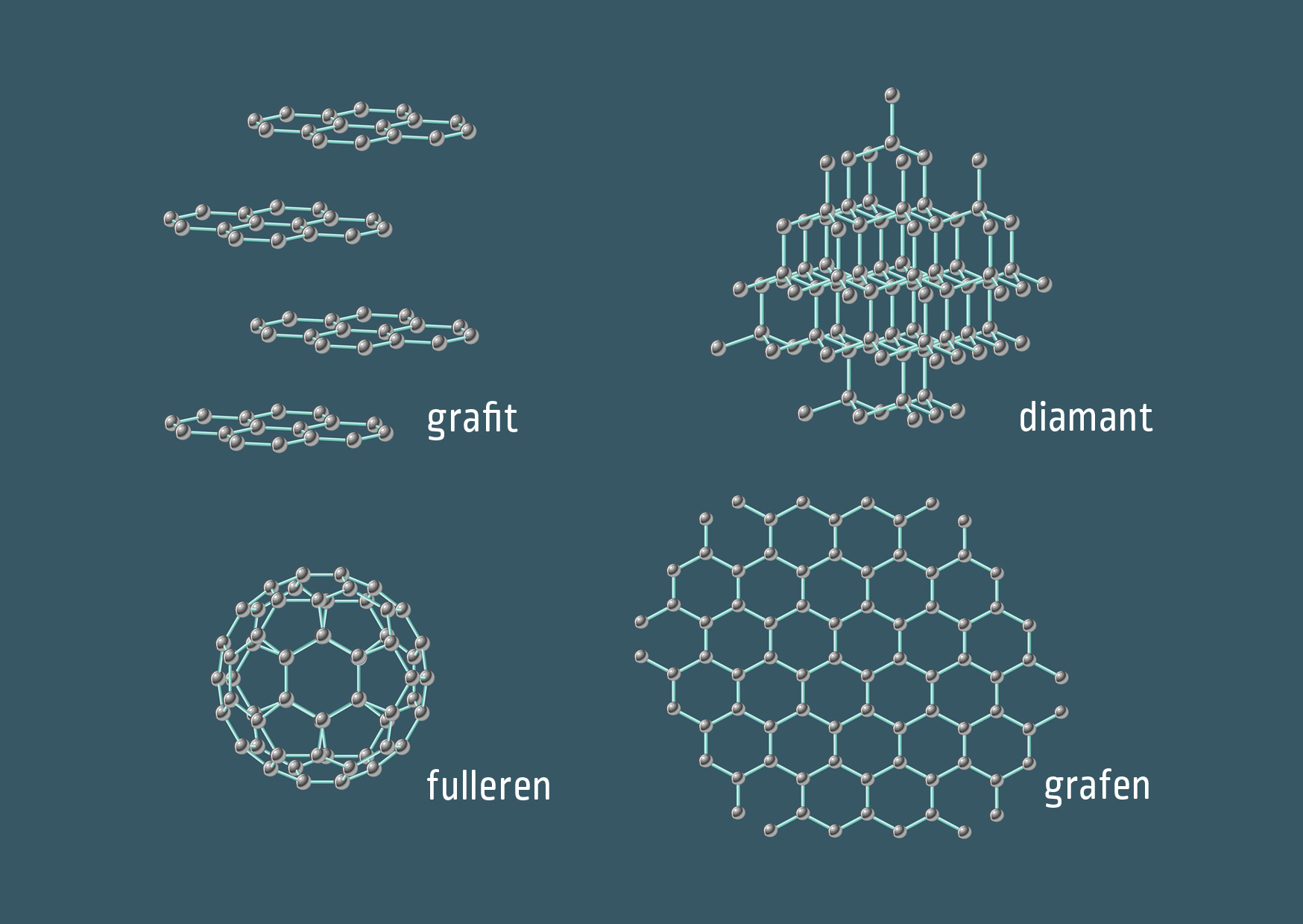
Zdroj
Mnohem důležitějším příkladem jsou ale různé typy ocelí. Ocel je pravděpodobně materiál s největší škálou dosažitelných mechanických vlastností. Čisté železo tuhne při teplotě 1538 °C a vytváří BCC mřížku (kubická prostorově centrovaná); této fázi se říká ferit. Po ochlazení pod 1394 °C se BCC mřížka mění v FCC (kubická plošně centrovaná) mřížku – austenit.
A při teplotách nižších než 912°C má rovnovážná fáze opět BCC mřížku (ferit). Chemickým legováním (např. přidáním niklu) je možné dosáhnout toho, že mřížka FCC je stabilní i za pokojové teploty. Pokud je v oceli přítomen uhlík, je možné rychlým ochlazením (zakalením) vytvořit martenzitickou fázi (tetragonální mřížka). Taková ocel je velmi pevná, ale také křehká. Tepelným zpracováním (kalením a popouštěním) lze „naladit“ pevnost a houževnatost na požadovanou hodnotu.
Obecně lze říci, že feritické oceli jsou levné, a proto se používají na velké konstrukce (nosníky budov, lodě, atd.). Je možné je zpevnit tepelným zpracováním, jsou magnetické; jedním z nežádoucích důsledků BCC mřížky je tzv. tranzitní chování, kdy s klesající teplotou feritické oceli křehnou a při teplotách cca −80 °C jsou křehké asi jako sklo. Problémem je také snadná koroze těchto ocelí.

Zdroj
Austenitické oceli jsou nemagnetické a při přidání Cr odolávají dobře korozi. Nerezavějící oceli, se kterými se běžně setkáváte (příbory, potravinářské nádoby, …), jsou austenitické. Nevykazují tranzitní chování, a používají se proto mj. i pro aplikace pracující za nízkých (kryogenních) teplot, například při zkapalňování zemního plynu a jeho přepravě.

Zdroj
Poruchy mříže a mechanické vlastnosti
Mechanické vlastnosti materiálů úzce souvisí s poruchami krystalové mříže. Je známé, že plastická (trvalá, nevratná) deformace krystalických materiálů je za běžných teplot způsobená pohybem čarových poruch – dislokací. Jde o pohyb celé jedné řady atomů, jak je znázorněno na následujícím dvourozměrném obrázku.

Zdroj
Zaznamenejme oblast elastické a plastické deformace do grafu deformační křivky.
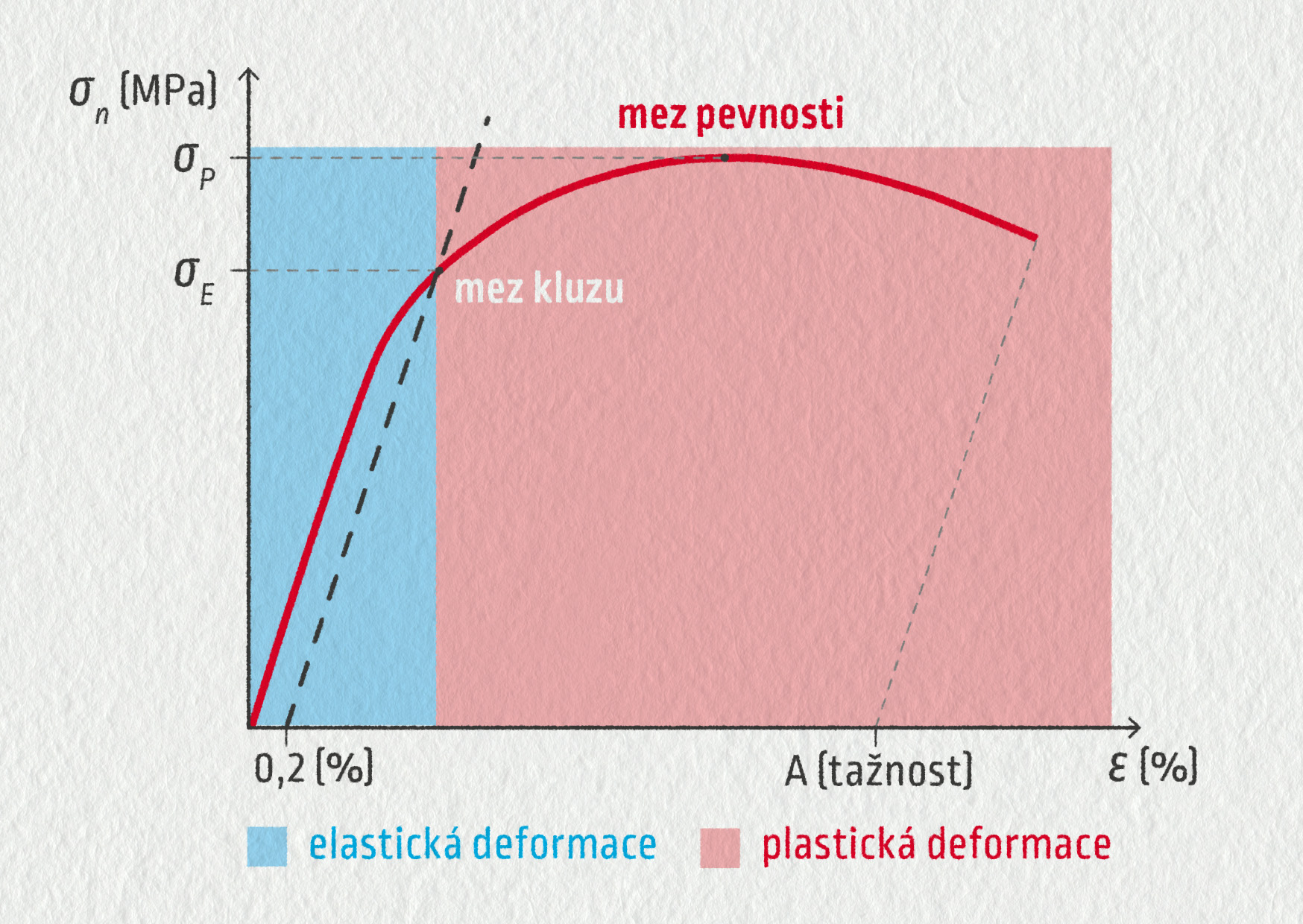
Zdroj
Obě oblasti jsou odděleny tzv. mezí kluzu. Jedná se o napětí, které je nutné k tomu, aby se dislokace v materiálu začaly pohybovat. Pokud je tento pohyb snadný (vyžíhané kovy), je mez kluzu nízká. Pokud je obtížný, jde o vysoce pevné materiály. Pokud je nemožný, materiál není schopen za dané teploty plastické deformace a je křehký. „Snadnost“, s jakou se dislokace pohybují mřížkou, je dána řadou faktorů:
- Pevností vazby: zejména kovalentní vazby (polovodiče) a iontové vazby (keramiky) jsou příliš pevné, aby se dislokace mohla za pokojové teploty pohybovat. K pohybu potřebuje pomoc tepelných kmitů mřížky (= tepelné aktivace); keramiky jsou proto tvárné až při teplotách přesahujících 1000 °C.
- Přidáním jiných atomů (substituční nebo intersticiální zpevnění) – přítomnost cizích atomů modifikuje chemické vazby a ztěžuje dislokacím pohyb.
- Zvýšením dislokační hustoty (deformační zpevnění) – množství dislokací v materiálu se může měnit o mnoho řádů. V materiálech s vysokou dislokační hustotou si dislokace vzájemně překážejí a k jejich pohybu je potřeba vyšší napětí. Zvýšit dislokační hustotu lze zejména tvářením za studena, tj. kováním, válcováním, protahováním apod.
- Zjemnění mikrostruktury – hranice zrn (tj. částí krystalů se stejnou orientací) nebo rozhraní mezi různými fázemi jsou pro dislokace překážkou. Zjemněním zrna nebo vytvořením lamelárních struktur lze výrazně zpevnit materiál.
- Přítomnost dalších fází (precipitační zpevnění) – malé precipitáty, tj. části materiálu s jiným chemickým složením a mřížkou, než je základní materiál, mohou velmi efektivně zpevnit materiál. Vyvinutí technologie vytvoření husté sítě precipitátů Al2Cu v hliníkových slitinách podstatně zvýšilo jejich pevnost a umožnilo rozvoj letectví.
Najděte v tabulkách teplotu tání, velikost Youngova modulu a rychlost šíření zvuku pro Fe, W, Ga, Al, Cu a diamant. Co můžeme usoudit o pevnosti vazeb u těchto prvků?
| Materiál | E (GPa) | TM (°C) | Rychlost zvuku (m/s) |
|---|---|---|---|
| Ga | 9,8 (20°C) | 30 | 2740 |
| Al | 70 | 660 | 5000 |
| Cu | 120 | 1085 | 3810 |
| Fe | 210 | 1538 | 5900 |
| W | 410 | 3422 | 5200 |
| C (diamant) | 1050 | 4027 | 18000 |
Je vidět, že \(E\) a \(T_\mathrm{M}\) spolu dobře korelují, obě vlastnosti jsou dány především pevností atomové vazby. U rychlosti zvuku je patrný trend, ale korelace není úplně dobrá, roli hrají další efekty než pouze pevnost vazby, zejména hmotnosti atomů. Lze usoudit, že vazba mezi atomy uhlíku je z daných příkladů nejpevnější.
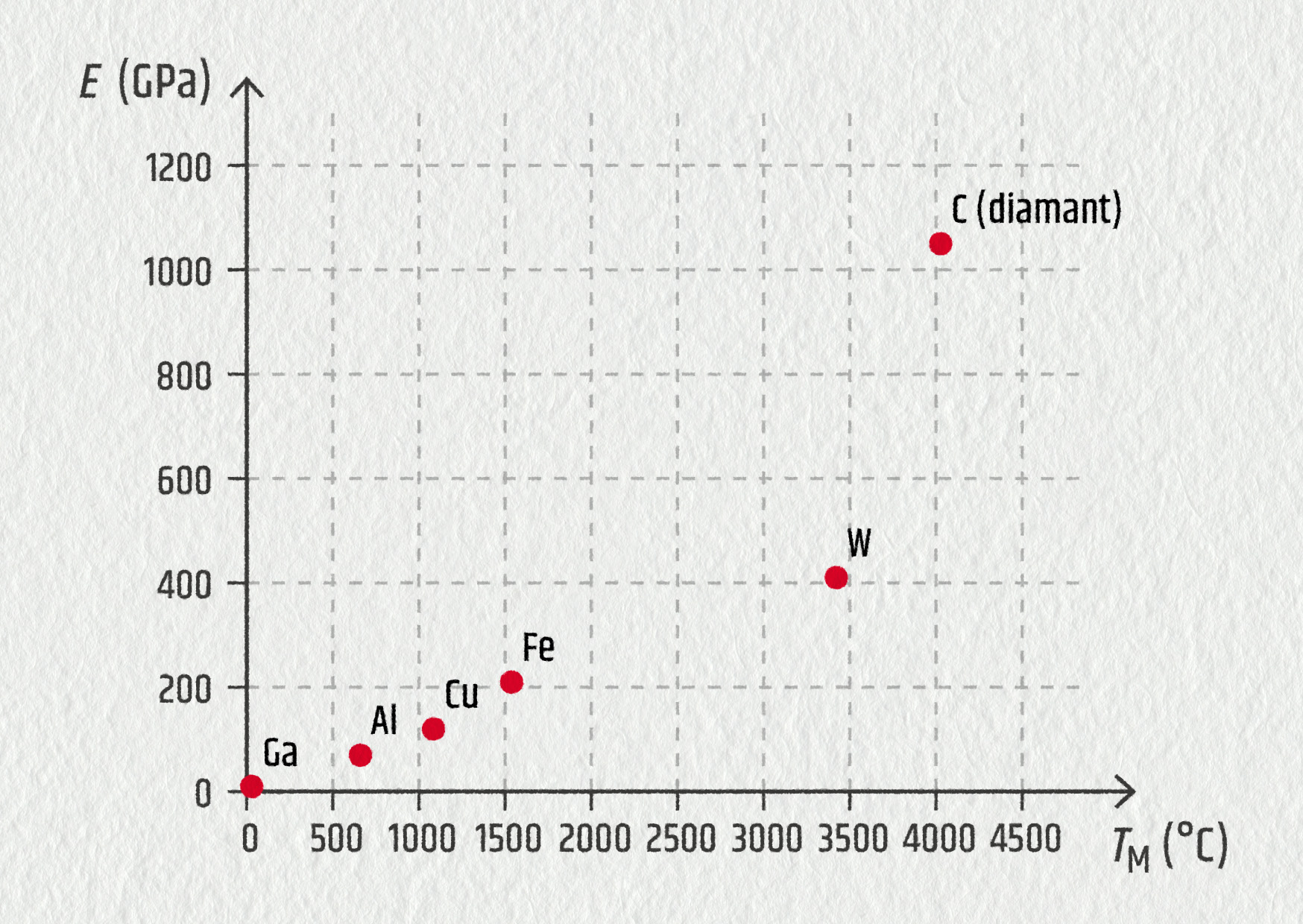
Zdroj
Poznámky
- často se nesprávně udává, že nejvyšší teplotu tání má wolfram;
- Youngův modul materiálů závisí na pevnosti vazby, a nelze ho tedy měnit; např. všechny typy ocelí mají E blízké 210 GPa;
- mez kluzu nemá tak jasnou spojitost s pevností vazby jako Youngův modul; je např. možné připravit ocel v široké škále pevností.
Kompozitní materiály
S rostoucím porozuměním vlastnostem různých materiálů se lidstvu daří využívat jejich vlastností lépe a lépe. Nebojíme se je kombinovat, a tím získat materiály, které jsou zároveň pevné i pružné, a to nám umožňuje jich využít například v lékařství, leteckém průmyslu nebo třeba ve stavebnictví.
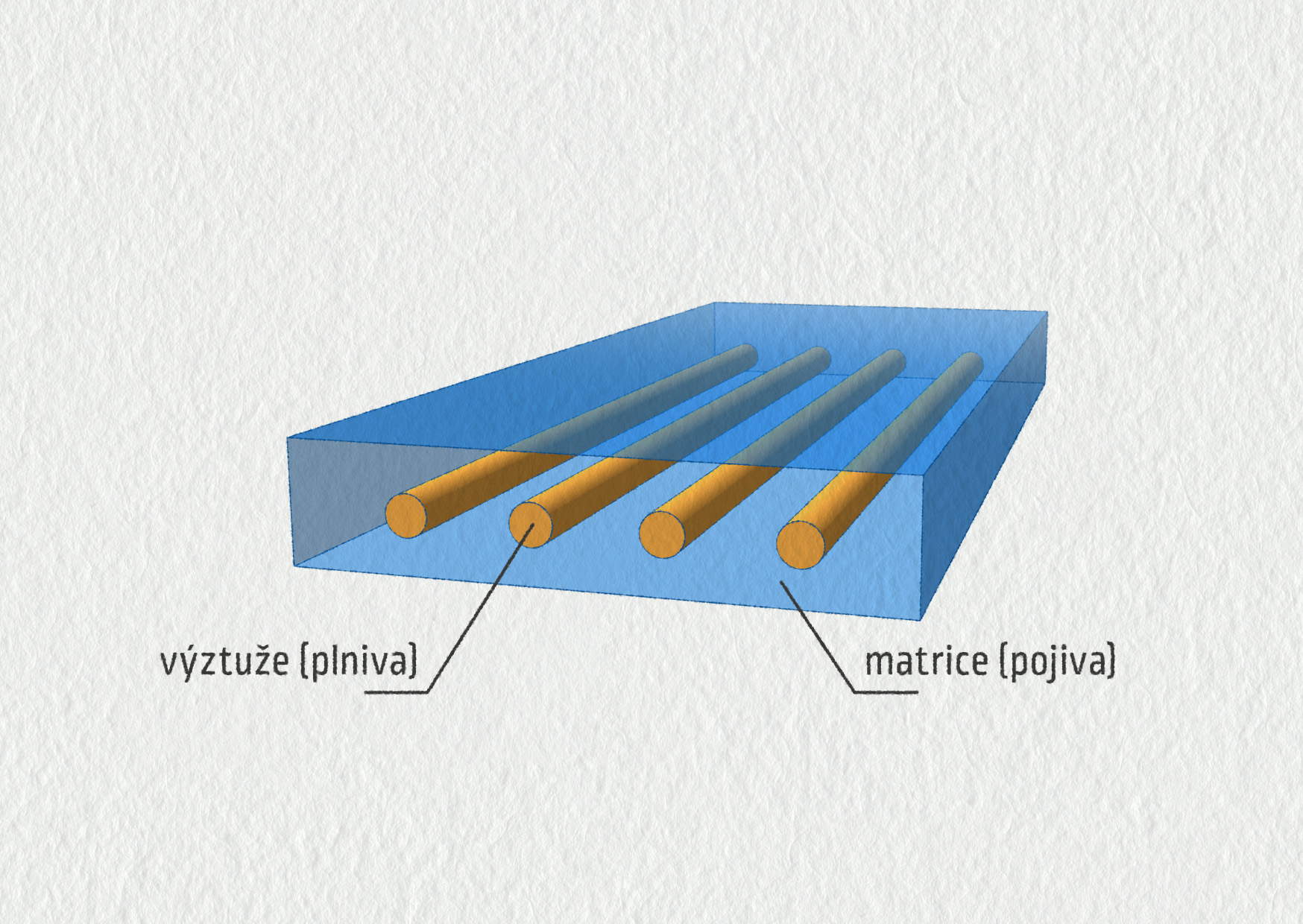
Kompozitní materiál je složen ze dvou nebo více různých materiálů (matricová a rozptýlená fáze – výztuže), které pevně spojíme. Tím docílíme lepších vlastností.
Zdroj
Hlavním úkolem matricové fáze je držet výztuže na místě, přenášet napětí v materiálu a chránit výztuže od okolí. Účel výztuže je různý: například kovy zvyšují tahové napětí materiálu (materiál je pevnější a odolnější proti namáhání), částice keramiky zase zajistí materiál, který odolává lomům, polymery zase umožní vytvořit pružnější materiál při zachování pevnosti.
Kompozitní materiály jsou zajímavou cestou, jak zlepšit vlastnosti materiálu. Jejich dalšímu rozšíření nyní brání především vyšší cena a zatím ne zcela vyřešená recyklace.
Kompozitní materiály

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj

Zdroj
Zdroj

Zdroj

